|
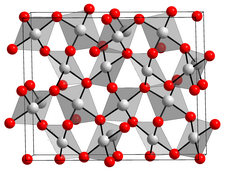
Oxyde d'or(III)
L'oxyde d'or(III), ou sesquioxyde d'or, est un composé chimique de formule Au2O3. C'est l'oxyde d'or le plus stable. Il s'agit d'un solide rouge brun cristallin semiconducteur[3] sensible à la lumière qui se décompose à 160 °C[4] en redonnant de l'or et de l'oxygène. En raison de la nature peu réactive de l'or, l'oxyde d'or(III) ne peut être obtenu par réaction directe de l'oxygène O2 sur l'or dans des conditions normales. Il peut cependant être produit par réaction de l'or avec l'oxygène en milieu aqueux sous pression de plusieurs milliers d'atmosphères, ou avec de l'oxygène à l'état plasma. Des cristaux d'oxyde d'or(III) peuvent être obtenus à partir de l'oxyde d'or(III) hydraté amorphe par réaction avec l'acide perchlorique HClO4 et un perchlorate ClO4− de métal alcalin dans un tube à quartz scellé à une température d'environ 250 °C et une pression de l'ordre de 30 MPa. Notes et références
|
||||||||||||||||||||||||||||||||||||||||||