|
Триметилсилилазид
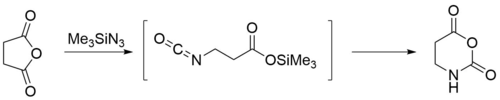
Триметилсилилазид — химическое соединение, алкил- и азидпроизводное моносилана с формулой (CH3)3SiN3, бесцветная жидкость. ПолучениеТриметилсилилазид получают кипячением триметилхлорсилана и азида натрия в дибутиловом эфире в течение 2 дней, после чего продукт перегоняют прямо из реакционного сосуда. Повторная перегонка позволяет получить триметилсилилазид с чистотой 99 %. Предложены также другие методики, где указанные компоненты вводятся в реакцию либо без растворителя, либо в более высококипящем растворителе (силиконовом масле или полиэтиленгликоле)[1]. Физические свойстваРастворяется в инертных органических растворителях. Химические свойства и применениеРеакции замещенияПод действием триметилсилилазида в органических растворителях бензил-, аллил- и незамещённые алкилгалогениды превращаются в соответствующие органические азиды. При добавлении хлорида олова(IV) в качестве катализатора в азиды превращаются также вторичные, третичные, циклические и полициклические галогениды. Позже спектр используемых галогенидов (а также фосфатов и тозилатов) был расширен благодаря использованию в качестве активатора фторида тетрабутиламмония[1]. Ацилгалогениды в реакциях с триметилсилилазидом превращаются в соответствующие ацилазиды, которые сразу вступают в перегруппировку Курциуса, давая изоцианаты. Однако в присутствии иодида цинка хлорангидриды ароматических кислот с высоким выходом дают ацилазиды[1]. Ортоэфиры и ацетали реагируют с триметилсилилазидом в присутствии хлорида олова(IV) при −78 °С, давая соответствующие азиды[1]. Реакции присоединенияВ присутствии хлорида цинка или хлорида олова(II) триметилсилилазид присоединяется к карбонильным соединениям, образуя α-триметилсилилоксиазиды. Альдегиды в эту реакцию вступают более активно, чем кетоны. Далее реакция в зависимости от условий приводит к диазидам, тетразолам или нитрилам[1]. Также триметилсилилазид присоединяется к оксиранам, давая β-триметилсилилоксиазиды, которые являются предшественниками β-аминоспиртов. Реакция катализируется хлоридом цинка, комплексами ванадия и титана, тартратом цинка и изопропоксидом алюминия. От катализатора зависит селективность процесса. Подобный процесс описан также для раскрытия азиридинов, которое позволяет получать 1,2-диамины[1]. При присоединении триметилсилилазида к ангидридам карбоновых кислот образуется равное количество силилового эфира и изоцианата. Циклические ангидриды также присоединяют триметилсилилазид, однако в их случае образуются ω-триметилсилилоксикарбонилизоцианаты, которые далее циклизуются 1,3-оксазин-2,6-дионы. Реакции циклоприсоединенияТриметилсилилазид присоединяется к алкинам по реакции [3+2]-диполярного циклоприсоединения, давая триазолы, а также к нитрилам — с образованием тетразолов[1]. БезопасностьТриметилсилилазид разлагается при 500 °С и является термически более стабильным, чем органические азиды. В холодильнике он хранится больше года. При контакте с водой он выделяет токсичную азотистоводородную кислоту, которая потенциально может вызывать вазодилатацию[1]. Примечания
Литература
Ссылки
Information related to Триметилсилилазид |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||





![{\displaystyle {\mathsf {ArCOX+Me_{3}SiN_{3}{\xrightarrow[{}]{ZnI_{2}}}ArCON_{3}+Me_{3}SiCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/83c79122420f92458bf3b4cce9650c6788d8988a)


![{\displaystyle {\mathsf {RR'C\!\!=\!\!O+Me_{3}SiN_{3}{\xrightarrow[{}]{ZnCl_{2}}}RR'N_{3}(OSiMe_{3}){\xrightarrow[{ZnCl_{2}}]{TMSA}}RR'C(N_{3})_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1ab781c1940b579147a0bd15a0f6abacac69a64f)