|
Condensation de KnoevenagelLa condensation de Knoevenagel est une réaction de chimie organique dans laquelle un composé carbonylé réagit avec un équivalent de carbanion en présence d'une base faible pour former un composé carbonylé α,β-insaturé ou un composé apparenté après élimination d'une molécule d'eau.  Avec Z un groupe électroattracteur, de type carbonyle, acide carboxylique, nitrile, ester, amide, phosphate, etc. HistoriqueEn 1894, Emil Knoevenagel découvre que la réaction entre le formaldéhyde et le malonate de diéthyle en présence de diéthylamine mène à la formation de l'adduit bis[1]. En 1896, il réussit à produire de l'acétoacétate d'éthylbenzylidène en faisant réagir du benzaldéhyde avec de l'acétoacétate d'éthyle[1]. MécanismeLe mécanisme est différent selon que la base ajoutée est une amine tertiaire d'une part, une amine primaire ou secondaire d'autre part[1]. Mécanisme de Hann-LapworthLe mécanisme est similaire à celui d'une condensation aldolique, l'amine tertiaire jouant le rôle de base en captant le proton en alpha des groupes électroattracteurs[1]. Mécanisme avec une amine secondaire ou primaireDans ce cas, l'amine réalise une addition nucléophile sur le composé carbonylé, conduisant après élimination d'un ion hydroxyde à un intermédiaire iminium qui est lui-même la cible d'une addition nucléophile menant aux produits[1]. UtilisationLa condensation de Knoevenagel est une étape importante de la synthèse de la luméfantrine, un principe actif anti-malaria qui entre dans la composition du coartem[2].  La synthèse du gaz CS comporte également une étape de condensation de Knoevenagel suivie de la réaction de la base avec l'adduit[3]. 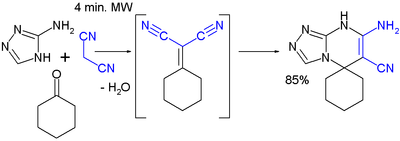 VariantesModification de DoebnerDans la modification de Doebner[4] de la condensation de Knoevenagel, l'équivalent de carbanion est l'acide malonique. Le produit initial peut alors subir une décarboxylation. La base employée est généralement la pyridine.  Réaction de Weiss-CookLa réaction de Weiss-Cook est la synthèse d'une cis-bicyclo[3.3.0]octane-3,7-dione à partir d'un diester dérivé de l'acétone et d'une 1,2-dicétone. Le mécanisme de cette réaction est semblable à celui de la condensation de Knoevenagel[5].  Notes et références
Information related to Condensation de Knoevenagel |